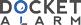`PATENTWESENS(PCT) VEROFFENTLICHTE INTERNATIONALE ANMELDUNG
`
`(19) Weltorganisationfiir geistiges Eigentum
`Internationales Biiro
`
`9, September 2005 (09.09.2005)
`
`(43) Internationales Veréffentlichungsdatum
`
`(10) Internationale Veréffentlichungsnummer
`WO 2005/083093 A2
`
`(51) Internationale Patentklassifikation’:
`;
`.
`(21) Internationales Aktenzeichen:
`(22) Internationales Anmeldedatum:
`23. Februar 2005 (23.02.2005)
`
`PCT/EP2005/001863
`
`C12N 15/82
`
`(25) Einreichungssprache:
`
`(26) Veréffentlichungssprache:
`(30) Angabenzur Prioritat:
`10 2004 009 457.8
`
`Deutsch
`
`Deutsch
`
`27. Februar 2004 (27.02.2004)
`
`DE
`
`10 2004 012 370.5
`10 2004 017 518.7
`10 2004 024 014.0
`PCT/EP/04/07957
`10 2004 062 543.3
`24. Dezember 2004 (24.12.2004) DE
`
`13. Marz 2004 (13.03.2004) DE
`8. April 2004 (08.04.2004) DE
`14. Mai 2004 (14.05.2004) DE
`16. Juli 2004 (16.07.2004)
`EP
`
`(71) Anmelder(fiir alle Bestimmungsstaaten mit Ausnahme von
`US): BASF PLANT SCIENCE GmbH [DE/DE]; 67056
`Ludwigshafen
`(DE).
`udwigshafen (DE)
`(72) Erfinder; und
`(75) Erfinder/Anmelder
`
`(nur fiir US): CIRPUS, Petra
`
`[Fortsetzung auf der ndchsten Seite]
`
`(54) Title: METHOD FOR PRODUCING POLYUNSATURATED FATTY ACIDS IN TRANSGENIC PLANTS
`
`(54) Bezeichnung: VERFAHREN ZUR HERSTELLUNG MEHRFACH UNGESATTIGTER FETTSAUREN IN TRANSGENEN
`PFLANZEN
`
`"
`Verschiedeno Synthese-Wege zur Blosynthese von DHA (Decosahexaensaure)
`
`B
`
`athwat
`pathway
`
`
`
`of
`oo
`— “ao-deseturase ewe
`sete PC —ek soap
`DoDii
`ypgsRare
`ggBNR goggatisnsr
`acca. setrene
`48-desaturasa
`“y”ee _
`
`oatsavs
`oease
`re
`
`
`. ascoagece
`Serecher
`oc
`cwae
`|
`.
`
`= |
`“aSedeseturese
`|
`Atslongase SS"
`eegeen
`Meets
`gong ShT404986 we pp.g ad710191619 q—_24:6 S002 a2
`aidesatuase”
`Boxidaion
`Dua
`
`
`
`A
`PKS
`ceca
`\|
`omerise
`:
`og M7H05848;9
`
`(57) Abstract: The invention relates to a method for producing
`.
`.
`:
`:
`polyunsaturated fatty acids in seeds of transgenic plants. According
`to said method, nucleic acids, coding for polypeptides with a
`@-3-desaturase, A-12-desaturase, A-6-desaturase, A-6-elongase,
`A-5-desaturase, A-S-elongase and/or A-4-desaturase activity,
`preferably for polypeptides with a A-6-desaturase, A-6-elongase
`and A-5-desaturase activity, are introduced into the organism. The
`nucleic acid sequencesare represented by SEQ ID NO:11, SEQ ID
`NO: 27, SEQ ID NO: 193, SEQ ID NO: 197, SEQ ID NO: 199 and
`SEQ ID NO:201. Advantageously, said nucleic acid sequences can
`be expressed in the organism optionally together with other nucleic
`acid sequences that code for polypeptides of the biosynthesis
`of the fatty acid or lipid metabolism. Nucleic acid sequences
`coding for a A-6-desaturase, A-5-desaturase, A-4-desaturase,
`A-1 2-desaturase and/or A-6-elongase activity are especially
`advantageous. Advantageously, said desaturases and elongases
`sos
`:
`:
`:
`:
`originate from thalassiosira, euglena or ostreococcus. The invention
`also relates to a method for producing oils and/or triacylglycerides with an increased content of long-chain polyunsaturated fatty
`acids. In a preferred embodiment, the invention also relates to a method for producing arachidonic acid, eicosapentaenic acid or
`docosahexaenic acid, and to a method for producing triglycerides with an increased content of unsaturated fatty acids, especially
`arachidonic acid, eicosapentaenoic acid and/or docosahexaenoic acid, in transgenic plants, preferably in seeds of the transgenic
`plants. The invention further relates to the production of a transgenic plant with an increased content of polyunsaturated fatty acids,
`especially arachidonic acid, eicosapentaenoic acid and/or docosahexaenoic acid, based on the expression of the elongases and
`desaturases used in the inventive method. The invention also relates to recombinant nucleic acids molecules containing, together
`or individually, nucleic acid sequences coding for the polypeptides with a A-6-desaturase, A-6-elongase, A-5-desaturase and
`A-5-elongase activity, and transgenic plants containing said recombinant nucleic acid molecules. Another part of the invention
`relates to oils, lipids and/or fatty acids produced according to the inventive method, and to the use thereof. Furthermore, the
`invention relates to unsaturated fatty acids and triglycerides with an increased content of unsaturated fatty acids, and to the use of
`the same.
`
`11... VARIOUS SYNTHESE-WAY FOR BIOSYNTHESE OF DHA (ACID DOCOSAHEXAENOIC)
`FF ... SPEAKER PATHWAY
`
`(57) Zusammenfassung: Die vorliegende Erfindungbetrifft ein Verfahren zur Herstellung von mehrfach ungesittigten Fettséuren
`im Samentransgener Pflanzen, indem Nukleinsaéuren in den Organismus eingebracht werden, die fiir Polypeptide mit w-3-Desa-
`turase-, A-12-Desaturase-, A-6-Desaturase-, A-6-Elongase-, A-5-Desaturase-, A-5-Elongase- und/oder A-4-Desaturaseaktivitat
`bevorzugt fiir Polypeptide mit A-6-Desaturase-,
`
`[Fortsetzung auf der ndchsten Seite]
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`083093A2IIfMITIMNIINUINIIIMINUNTITMTMAUINTACGAT
`
`=S
`
`o ©S
`
`
`
`WO 2005/083093 A2
`
`[DE/DE]; Landteilstr.12, 68163 Mannheim (DE). BAUER,
`Jérg [DE/DE]; Thorwaldsenstr. 1A, 67061 Ludwigshafen
`(DE). QIU, Xiao [CA/CA]; 403 Kendardine Road, Saska-
`toon Sk. S7N 385 (CA). WU, Guohai [CA/CA]; 2103
`Kenderdine Road, Saskatoon Sk. S7N 4A9 (CA). DATLA,
`Nagamani [CA/CA]; 527 Bayview Terrace, Saskatoon Sk.
`S7V 1B6 (CA).
`
`c/o BASF Aktienge-
`PRESSLER, Uwe;
`(74) Anwalt:
`sellschaft, 67056 Ludwigshafen (DE).
`
`(81) Bestimmungsstaaten (soweit nicht anders angegeben, fiir
`jede verfiigbare nationale Schutzrechtsart): AE, AG, AL,
`AM,AT, AU, AZ, BA, BB, BG, BR, BW,BY, BZ, CA, CH,
`CN, CO, CR, CU, CZ, DE, DK, DM,DZ,EC, EE, EG, ES,
`FI, GB, GD, GE, GH, GM,HR, HU,ID,IL,IN,IS, JP, KE,
`KG,KP, KR, KZ, LC, LK, LR, LS, LT, LU, LV, MA, MD,
`MG,MK, MN, MW,Mx,MZ,NA,NI, NO, NZ, OM,PG,
`PH,PL, PT, RO, RU, SC, SD, SE, SG, SK, SL, SM,SY, TJ,
`
`TM,TN,TR, TT, TZ, UA, UG, US, UZ, VC, VN, YU, ZA,
`ZM, ZW.
`
`(84) Bestimmungsstaaten (soweit nicht anders angegeben, fiir
`jede verfiigbare regionale Schutzrechtsart): ARIPO (BW,
`GH, GM, KE, LS, MW, MZ, NA, SD, SL, SZ, TZ, UG,
`ZM, ZW), eurasisches (AM, AZ, BY, KG, KZ, MD, RU,
`TJ, TM), europaisches (AT, BE, BG, CH, CY, CZ, DE, DK,
`EE, ES, FI, FR, GB, GR, HU,IE,IS, IT, LT, LU, MC, NL,
`PL, PT, RO, SE, SI, SK, TR), OAPI (BF, BJ, CF, CG, CI,
`CM, GA, GN, GQ, GW, ML, MR, NE, SN, TD, TG).
`
`Veroffentlicht:
`ohne internationalen Recherchenbericht und erneut zu ver-
`Offentlichen nach Erhalt des Berichts
`
`Zur Erkldrung der Zweibuchstaben-Codes und der anderen Ab-
`kiirzungen wird auf die Erkldrungen ("Guidance Notes on Co-
`des and Abbreviations") am Anfang jeder reguldren Ausgabe der
`PCT-Gazette verwiesen.
`
`A-6-Elongase- und A-5-Desaturaseaktivitat codieren. Bei den Nukleinsauresequenzen handelt es sich um die in SEQ ID NO: 11,
`SEQ ID NO: 27, SEQ ID NO: 193, SEQ ID NO: 197, SEQ ID NO: 199 und SEQ ID NO: 201 dargestellten Sequenzen. Vorteil-
`haft kénnen diese Nukleinséuresequenzen gegebenenfalls zusammen mit weiteren Nukleinséuresequenzen, die fiir Polypeptide der
`Biosynthese des Fettsaure- oder Lipidstoffwechels codieren, in dem Organismus exprimiert werden. Besonders vorteilhaft sind Nuk-
`leinsdiuresequenzen,die fiir eine A-6-Desaturase-, eine A-5-Desaturase-, A-4-Desaturase-, A-1 2-Desaturase- und/oder A-6-Elon-
`gaseaktivitat codieren. Vorteilhaft stammen diese Desaturasen und Elongasen aus Thalassiosira, Euglena oder Ostreococcus. Weiter-
`hin betrifft die Erfindung ein Verfahren zur Herstellung von Olen und/oder Triacylglyceriden mit einem erhéhten Gehalt an langket-
`tigen mehrfach ungesattigten Fettsaéuren. Die Erfindungbetrifft in einer bevorzugten Ausfithrungsform ausserdem ein Verfahren zur
`Herstellung von Arachidonsdure, Eicosapentaenséure oder Docosahexaensdure sowie ein Verfahren zur Herstellung von Triglyceri-
`den mit einem erhéhten Gehalt an ungesattigten Fettsduren, insbesondere Arachidonsdure, Eicosapentaensaure und/oder Docosa-
`hexaensdure, in transgenen Pflanzen vorteilhaft im Samen der transgenen Pflanze. Die Erfindung betrifft die Herstellung einer
`transgenen Pflanze mit erhédhtem Gehalt an mehrfach ungesattigten Fettsduren, insbesondere Arachidonsdure, Eicosapentaensdure
`und/oder Docosahexaensaure, aufgrund der Expression der im erfindungsgeméssen Verfahren verwendeten Elongasen und Desat-
`urasen. Die Erfindung betrifft weiterhin rekombinante Nukleinsaéuremolekiile, die die Nukleinsaéuresequenzen,die fiir die Polypep-
`tide mit A-6-Desaturase-, A-6-Elongase-, A-5-Desaturase- und A-5-Elongaseaktivitét kodieren, gemeinsam odereinzeln enthalten,
`sowie transgene Pflanzen, die die vorgenannten rekombinanten Nukleinsaéuremolekiile enthalten. Ein weiterer Teil der Erfindung
`betrifft Ole, Lipide und/oder Fettstiuren hergestellt nach dem erfindungsgemiissen Verfahren und deren Verwendung. Ausserdem
`betrifft die Erfindung ungesattigte Fettsduren sowie Triglyceride mit einem erhdéhten Gehalt an ungesattigten Fettsauren und deren
`Verwendung.
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO2005/083093
`
`PCT/EP2005/001863
`
`Verfahren zur Herstellung mehrfach ungesattigter Fettsauren in transgenen
`Pflanzen
`
`Beschreibung:
`
`Die vorliegende Erfindung betrifft ein Verfahren zur Herstellung von mehrfach unge-
`sattigten Fettsauren im Samentransgener Pflanzen, indem Nukieinsauren in den
`Organismus eingebracht werden, die fur Polypeptide mit w-3-Desaturase-, A-12-
`Desaturase-, A-6-Desaturase-, A-6-Elongase-, A-5-Desaturase-, A-5-Elongase-
`und/oder A-4-Desaturaseaktivitat bevorzugt fir Polypeptide mit A-6-Desaturase-, A-6-
`Elongase- und A-5-Desaturaseaktivitat codieren.
`
`10
`
`15
`
`Bei den Nukleinsduresequenzen handelt es sich um die in SEQ ID NO:11, SEQ ID
`NO: 27, SEQ ID NO: 193, SEQ ID NO: 197, SEQ ID NO: 199 und SEQ ID NO: 201
`dargestellten Sequenzen. Bevorzugt wird neben diesen Nukleinsauresequenzen eine
`weitere Nukleinsauresequenz,die fir ein Polypeptid mit einer A-12-Desaturaseaktivitat
`kodiert, in die Pflanze eingebracht und ebenfalls gleichzeitig exprimiert. Besonders
`bevorzugt handelt es sich dabei um die in SEQ ID NO: 195 dargestellte Nukleinsaure-
`sequenz.
`
`20 ©
`
`25
`
`30
`
`35
`
`Vorteilhaft konnen diese Nukleinsauresequenzen gegebenenfalls zusammen mit
`weiteren Nukleinsauresequenzen, die fur Polypeptide der Biosynthese des Fettsaure-
`oderLipidstoffwechels codieren, in dem Organismus exprimiert werden. Besonders
`vorteilhaft sind Nukleinsauresequenzen,die fireine A-6-Desaturase-, eine A-5-
`Desaturase-, A-4-Desaturase-, A-12-Desaturase- und/oder A-6-Elongaseaktivitat
`codieren. Vorteilhaft stammen diese Desaturasen und Elongasen aus Thalassiosira,
`Euglena oder Ostreococcus. Weiterhin betrifft die Erfindung ein Verfahren zur Herstel-
`lung von Olen und/oderTriacylglyceriden mit einem erhohten Gehalt an langkettigen
`mehrfach ungesattigten Fettsauren.
`
`__
`
`Die Erfindungbetrifft in einer bevorzugten Ausfiihrungsform auferdem ein Verfahren
`zur Herstellung von Arachidonsdure, Eicosapentaensaure oder Docosahexaensaure
`sowie ein Verfahren zur Herstellung von Triglyceriden mit einem erhéhten Gehalt an
`ungesattigten Fettsauren, insbesondere Arachidonsaure, Eicosapentaensaure
`und/oder Docosahexaensdure,in transgenen Pflanzen vorteilhaft im Samen der
`transgenen Pflanze. Die Erfindung betrifft die Herstellung einer transgenen Pflanze mit
`erhéhtem Gehalt an mehrfach ungesattigten Fettsauren, insbesondere Arachidonsau-
`re, Eicosapentaensaure und/oder Docosahexaensaure, aufgrund der Expression der
`im erfindungsgemaRen Verfahren verwendeten Elongasen und Desaturasen.
`
`Die Erfindungbetrifft weiterhin rekombinante Nukleinsauremolekile, die die Nuklein-
`sduresequenzen,die fur die Polypeptide mit A-6-Desaturase-, A-6-Elongase-, A-5-
`Desaturase- und A-5-Elongaseaktivitat kodieren, gemeinsam odereinzein enthalten,
`sowie transgene Pflanzen, die die vorgenannten rekombinanten Nukleinsauremolekile
`enihalten.
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO2005/083093
`
`PCT/EP2005/001863
`
`2
`
`.
`
`Ein weitererTeil der Erfindung betrifft Ole, Lipide und/oder Fettsauren hergestellt
`nach dem erfindungsgemaGen Verfahren und deren Verwendung. Auerdem betrifft
`die Erfindung ungesattigte Fettsauren sowie Triglyceride mit einem erhéhten Gehalt an
`ungesattigten Fettsauren und deren Verwendung.
`
`Die Lipidsynthese lasst sich in zwei Abschnitte unterteilen: die Synthese von Fettsau-
`ren und ihre Bindung an sn-Glycerin-3-Phosphat sowie die Addition oder Modifikation
`einer polaren Kopfgruppe. Ubliche Lipide, die in Membranen verwendet werden,
`umfassen Phospholipide, Glycolipide, Sphingolipide und Phosphoglyceride. Die
`Fettsauresynthese beginnt mit der Umwandlung von Acetyl-CoA in Malonyl-CoA durch
`die Acetyl-CoA-Carboxylase oderin Acetyl-ACP durch die Acetyltransacylase. Nach
`einer Kondensationsreaktion bilden diese beiden Produktmolekiile zusammen Aceto-
`acetyl-ACP, das iber eine Reihe von Kondensations-, Reduktions- und Dehydratisie-
`rungsreaktionen umgewandelt wird, so dass ein gesattigtes Fettsauremolekil mit der
`gewinschten Kettenlange erhalten wird. Die Produktion der ungesattigten Fetisauren
`aus diesen Molekiilen wird durch spezifische Desaturasen katalysiert, und zwar
`entwederaerob mittels molekularem Sauerstoff oder anaerob (beziiglich der Fett-
`' sauresynthese in Mikroorganismensiehe F.C. Neidhardtet al. (1996) E. coli und
`Salmonella. ASM Press: Washington, D.C., S. 612-636 und darin enthaltene Literatur-
`stellen; Lengeleret al. (Hrsgb.) (1999) Biology of Procaryotes. Thieme: Stuttgart, New
`York, und die enthalteneLiteraturstellen, sowie Magnuson, K., et al. (1993) Microbiolo-
`gical Reviews 57:522-542 und die enthaltenenLiteraturstellen). Die so hergestellten an
`Phospholipide gebundenen Fettsauren miissen anschlieRend fir die weiteren Elonga-
`tionen aus den Phospholipiden wiederin den FettsaureCoA-Ester-Pool Uberfihrt
`werden. Dies erméglichen Acyl-CoA:Lysophospholipid-Acyltransferasen. Weiterhin
`kénnen diese Enzymedie elongierten Fettsauren wieder von den CoA-Estern aufdie
`Phospholipide tibertragen. Diese Reaktionsabfolge kann gegebenenfalls mehrfach
`durchlaufen werden.
`
`_
`
`Ferner miissen Fettsauren anschlie&end an verschiedene Modifikationsorte transpor-
`tiert und in das Triacylglycerin-Speicherlipid eingebaut werden. Ein weiterer wichtiger
`Schritt bei der Lipidsynthese ist der Transfer von Fettsauren auf die polaren Koptf-
`gruppen, beispielsweise durch Glycerin-Fettsaure-Acyltransferase (siehe Frentzen,
`1998, Lipid, 100(4-5):161-166).
`
`Verdéffentlichungen Uber die Pflanzen-Fettsaurebiosynthese, Desaturierung, den Lipid-
`stoffwechsel und Membrantransport vonfetthaltigen Verbindungen, die Betaoxidation,
`Fettsauremodifikation und Cofaktoren, Triacylglycerin-Speicherung und -
`Assemblierung einschlie@lich der Literaturstellen darin siehe in den folgenden Artikeln:
`Kinney, 1997, Genetic Engeneering, Hrsgb.: JK Setlow, 19:149-166; Ohlrogge und
`Browse, 1995, Plant Cell 7:957-970; Shanklin und Cahoon, 1998, Annu. Rev. Plant
`Physiol. Plant Mol. Biol. 49:611-641; Voelker, 1996, Genetic Engeneering, Hrsgb.: JK
`Setlow, 18:111-13; Gerhardt, 1992, Prog. Lipid R. 31:397-417; Gihnemann-Schafer &
`Kindl, 1995, Biochim. Biophys Acta 1256:181-186; Kunau et al., 1995, Prog. Lipid Res.
`34:267-342; Stymneet al., 1993, in: Biochemistry and Molecular Biology of Membrane
`
`10
`
`15
`
`20
`
`25
`
`30
`
`35
`
`40
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO2005/083093
`
`PCT/EP2005/001863
`
`3
`
`and Storage Lipids of Plants, Hrsgb.: Murata und Somerville, Rockville, American
`Society of Plant Physiologists, 150-158, Murphy & Ross 1998, Plant Journal. 13(1):1-
`16.
`
`Im folgenden werden mehrfach ungesattigteFettsauren als PUFA, PUFAs, LCPUFA
`oder LCPUFAs bezeichnet(poly unsaturated fatty acids, PUFA, mehrfach ungesattigte
`Fettsauren;long cchain poly uiunsaturated fatty acids, LCPUFA,langkettige mehrfach
`ungesattigte Fettsauren).
`
`Fettsauren und Triacylglyceride haben eine Vielzahl von Anwendungenin der
`Lebensmittelindustrie, der Tierernahrung, der Kosmetik und im Pharmabereich.
`Je nachdem, ob essich um freie gesattigte und ungesattigte Fettsauren. oder um
`- Triacylglyceride mit einem erhéhten Gehalt an gesattigten oder‘ungesattigten Fett-
`sduren handelt, sind sie fur die unterschiedlichsten Anwendungengeeignet. Mehrfach-
`ungesattigte Fettsauren wie Linol- und Linolensauresind fur Saugetiere essentiell,
`da sie nicht von diesen selbst hergestellt werden kénnen. Deshalbstellen mehrfach
`ungesattigte w-3-Fettsauren und w-6-Fettsauren einen wichtigen Bestandteil der
`tierischen und menschlichen Nahrung dar. So werdenz.B. in der humanen Ernahrung
`Lipide mit ungesattigten Fettsauren, speziell mehrfach ungesaitigten, Fettsauren
`bevorzugt. Den mehrfach ungesattigten w-3-Fettsauren wird dabei ein positiver Effekt
`auf den Cholesterinspiegel im Blut und damit auf die Pravention einer Herzerkrankung
`zugeschrieben. Durch Zugabe dieser w-3-Fettsauren zur Nahrung kann das Risiko
`_einer Herzerkrankung, eines Schlaganfalls oder von Bluthochdruck deutlich verringert
`werden (Shimikawa 2001, World Rev.Nutr. Diet. 88, 100-108).
`
`Auch entztindliche, speziell chronisch entziindliche, Prozesse im Rahmen immunologi-
`scher Erkrankungen wie rheumatoiderArthritis lassen sich durch w~3-Fettsauren
`positiv beeinflussen (Calder 2002, Proc. Nutr. Soc. 61, 345-358; Cleland und James
`2000, J. Rheumatol. 27, 2305-2307). Sie werden deshalb Lebensmitteln, speziell
`didtetischen Lebensmitteln, zugegeben oderfinden in Medikamenten Anwendung. w-6-
`Fettsauren wie Arachidonsaure Uben bei diesen rneumatischen Erkrankungen eher
`einen negativen Effekt aus.
`
`w)-3- und w-6-Fettsauren sind Vorlaufer von Gewebshormonen, den sogenannten
`Eicosanoiden wie den Prostaglandinen, die sich von der Dihomo-y-linolensaure,
`der Arachidonsaure und der Eicosapentaensaure ableiten, und den Thromboxanen
`und Leukotrienen, die sich von der Arachidonsaure und der Eicosapentaensaure
`ableiten. Eicosanoide (sog. PG2-Serie), die aus w-6-Fettsauren gebildet werden,
`fordern in der Regel Entztindungsreaktionen, wahrend Eicosanoide (sog. PG;-Serie)
`aus W-3-Fettsauren geringe oder keine entztindungsférdernde Wirkung haben.
`
`Mehrfach ungesattigte langkettige w-3-Fettsauren wie Eicosapentaensaure (= EPA,
`620:5%8:14:14.17) oder Docosahexaensdure (= DHA, C22:6447'9"5":"°) sind wichtige
`Komponenten der menschlichen Ernahrung aufgrundihrer verschiedenen Rollen in der
`Gesundheit, die Aspekte wie die Entwicklung des kindlichen Gehirns, der Funktionalitat
`des Auges, der Synthese von Hormonenund andererSignalstoffe, sowie die Vorbeu-
`
`10°
`
`15
`
`20
`
`25
`
`30
`
`35
`
`40
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`. WO2005/083093
`
`PCT/EP2005/001863
`
`4
`gung von Herz-Kreislauf-Beschwerden, Krebs und Diabetes umfassen (Poulos, A
`Lipids 30:1-14, 1995; Horrocks, LA und Yeo YK Pharmacol Res 40:211-225, 1999). Es
`besteht aus diesem Grund ein Bedarf an der Produktion mehrfach ungesattigter
`langkettiger Fettsauren.
`
`Aufgrund der heute ublichen Zusammensetzung der menschlichen Nahrungist ein
`Zusatz von mehrfach ungesaitigten w-3-Fettsauren, die bevorzugt in Fischélen
`vorkommen, zur Nahrung besonders wichtig. So werden beispielsweise mehrfach
`ungesattigte Fettsauren wie Docosahexaensaure (= DHA, C22:6%*7"'9"°:"°) oder
`Eisosapentaensaure (= EPA, C20:5%°8"""417) Babynahrung zur Erhéhung des
`Nahrwertes zugesetzt. Der ungesaittigten Fettsaure DHA wird dabeiein positiver Effekt
`auf die Entwicklung und Aufrechterhaltung von Gehirnfunktionen zugeschrieben. Es
`besteht aus diesem Grund ein Bedarf an der Produktion mehrfach ungesattigter
`langkettiger Fettsauren. -
`
`Hauptsachlich werden die verschiedenen Fettsauren und Triglyceride aus Mikro-
`organismenwie Mortierella oder Schizochytrium oder aus Ol-produzierenden Pflanzen
`wie Soja, Raps, Algen wie Crypthecodinium oder Phaeodactylum und weiteren ge-
`wonnen, wobeisie in der Regel in Form ihrer Triacylglyceride (= Triglyceride = Tri-
`glycerole) anfallen. Sie kénnen aber auch aus Tieren wiez.B. Fischen gewonnen
`werden.Die freien Fettsauren werdenvorteilhaft durch Verseifung hergestellt. Sehr
`langkettige mehrfach ungesattigte Fettsauren wie DHA, EPA, Arachidonsaure (= ARA,
`C20:44%8144) Dinomo-y-linolensaure (C20:3°°"*"*) oder Docosapentaensaure (DPA,
`622:5471'3.18.18) werden in Olfruchtpflanzen wie Raps, Soja, Sonnenblume, Farber-
`saflor nicht synthetisiert. Ubliche natirliche Quellen fiir diese Fettsauren sind Fische
`wie Hering, Lachs, Sardine, Goldbarsch, Aal, Karpfen, Forelle, Heilbutt, Makrele,
`Zanderoder Thunfisch oder Algen.
`
`Je nach Anwendungszweck werden Ole mit gesattigten oder ungesattigten Fettsauren
`bevorzugt. So werden z.B. in der humanen Ernahrung Lipide mit ungesattigten Feit-
`sduren speziell mehrfach ungesattigten Fettsauren bevorzugt. Den mehrfach unge-
`sattigten w-3-Fettsduren wird dabeiein positiver Effekt auf den Cholesterinspiegel
`im Biut und damit auf die Méglichkeit der Pravention einer Herzerkrankung zuge-
`schrieben. Durch Zugabe dieser w-3-Fettsauren zur Nahrung kann das Risiko einer
`Herzerkrankung, eines Schlaganfalls oder von Bluthochdruck deutlich verringert
`werden. Auch entztindliche speziell chronisch entziindliche Prozesse im Rahmen
`immunologischer Erkrankungen wie rheumatroiderArthritis lassen sich durch w-3-
`Fettsdurenpositiv beeinflussen. Sie werden deshaib Lebensmitteln speziell diatischen
`Lebensmitteln zugegeben oderfinden in Medikamenten Anwendung. w-6-Fettsauren
`wie Arachidonsdure habenbei diesen rheumatischen Erkrankungen aufgrund unserer
`Ublichen Nahrungsmittelzusammensetzung ehereinen negativen Effekt auf diese
`Krankheiten.
`
`10
`
`15
`
`20
`
`25
`
`30
`
`35
`
`40
`
`Aufgrundihrer positiven Eigenschaften hat es in der Vergangenheit nicht an Ansatzen
`gefehit, Gene, die an der Synthese von Fettsauren bzw.Triglyceriden beteiligt sind, far
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO2005/083093
`
`PCT/EP2005/001863
`
`5
`
`die Herstellung von Olen in verschiedenen Organismen mit geandertem Gehalt an
`ungesattigten Fettsauren verfugbar zu machen. So wird in WO 91/13972 und seinem
`US—Aquivalent eine A~9~-Desaturase beschrieben. In WO 93/11245 wird eine A-15—
`Desaturase in WO 94/11516 wird eine A-12—Desaturase beansprucht. Weitere
`Desaturasen werden beispielsweise in EP—A-0 550 162, WO 94/18337, WO 97/30582,
`WO 97/21340, WO 95/18222, EP~A-0 794 250, Stukeyetal., J. Biol. Chem., 265,
`41990: 20144-20149, Wada et al., Nature 347, 1990: 200-203 oder Huang et al., Lipids
`34, 1999: 649-659 beschrieben. Die biochemische Charakterisierung der verschie-
`denen Desaturasenist jedoch bisher nur unzureichend erfolgt, da die Enzyme als
`membrangebundeneProteine nur sehr schwerzu isolieren und zu charakterisieren
`sind (McKeonet al., Methods in Enzymol. 71, 1981: 12141-12147, Wang etal., Plant
`Physiol. Biochem., 26, 1988: 777-792). In der Regelerfolgtdie Charakterisierung
`membrangebundener Desaturasen durch Einbringungin einen geeigneten Organis-
`_mus, der anschlieBend auf Enzymaktivitat mittels Edukt- und Produktanalyse unter-
`sucht wird. A~6—Desaturasen werden in WO 93/06712, US 5,614,393, US5614393,
`WO 96/21022, WO00/21557 und WO 99/27111 beschrieben. Die Anwendung zur
`Produktion in transgenen Organismenwird in WO98/46763 WO98/46764, WO9846765
`beschrieben. Die Expression verschiedener Desaturasen wird in WO99/64616 oder
`WO98/46776 beschrieben und beansprucht. Bzgl. der Effektivitat der Expression von
`Desaturasen und ihrem Einfluss auf die Bildung mehrfach ungesattigterFettsaurenist
`anzumerken, dass durch Expression einer einzelnen Desaturase wie bisher beschrie-
`_ benlediglich geringe Gehalte an ungesattigten Fettsauren/Lipidenvwie z.B. y-
`Linolensaure und Stearidonsaureerreicht wurden.
`In der Vergangenheit wurden zahlreiche Versuche unternommen, Elongase-Gene
`zu erhalten. Millar and Kunst, 1997 (Plant Journal 12:121-131) und Millar et al., 1999
`(Plant Cell 11:825-838) beschreiben die Charakterisierung von pflanzlichen Elongasen
`zur Synthese von einfach ungesattigten langkettigen Fettsauren (C22:1) bzw. zur
`Synthese vonsehrlangkettigen Fettsauren fur die Wachsbildung in Pflanzen (C2—-C32).
`Beschreibungen zur Synthese von Arachidonsaure und EPAfindensich beispielsweise
`in WO 01/59128, WO 00/12720, WO 02/077213 und WO 02/08401. Die Synthese von
`mehrfach ungesattigter C24-Fettsauren ist beispielsweise in Tvrdik et al. 2000, J. Cell
`- Biol. 149:707-718 oder WO 02/44320 beschrieben.
`
`Besonders geeignete Mikroorganismen zur Herstellung von PUFAssind Mikro-
`organismen wie Mikroalgen wie Phaeodactylum tricornutum, Porphiridium-Arten,
`Thraustochytrien-Arten, Schizochytrien-Arten oder Crypthecodinium-Arten,Ciliaten,
`wie Stylonychia oder Colpidium,Pilze, wie Mortierella, Entomophthora oder Mucor
`und/oder Moosen wie Physcomitrella, Ceratodon und Marchantia (R. Vazhappilly & F.
`Chen (1998) Botanica Marina 41: 553-558; K. Totani & K. Oba (1987) Lipids 22: 1060-
`1062: M. Akimoto et al. (1998) Appl. Biochemistry and Biotechnology 73: 269-278).
`Durch Stammselektion ist eine Anzahl von Mutantenstammen der entsprechenden
`Mikroorganismen entwickelt worden, die eine Reihe wiinschenswerter Verbindungen,
`einschlieBlich PUFAs, produzieren. Die Mutation und Selektion von Stammen mit
`verbesserter Produktion eines bestimmten Molekiils wie den mehrfach ungesaitigten
`
`10
`
`15
`
`20°
`
`25
`
`30
`
`35
`
`40
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO2005/083093
`
`PCT/EP2005/001863
`
`6
`
`Fettsauren ist jedoch ein zeitraubendes und schwieriges Verfahren. Deshalb werden,
`wann immer méglich wie oben beschrieben gentechnologische Verfahren bevorzugt.
`Mit Hilfe der vorgenannten Mikroorganismenlassen sich jedoch nur begrenzte Mengen
`der gewiinschten mehrfach ungesattigten Fettsauren wie DPA, EPA oder ARA her-
`stellen. Wobei diese in der Regel je nach verwendeten Mikroorganismusals Fettsaure-
`gemische aus beispielsweise EPA, DPA und ARA anfallen.:
`
`Hdhere Pflanzen enthalten mehrfach ungesattigte Fettsauren wie Linolsaure (C18:2)
`und Linolensaure (C18:3). ARA, EPA und DHA kommen im Samendl héherer Pflanzen
`gar nicht oder nur in Spuren vor (E. Ucciani: Nouveau Dictionnaire des Huiles Végé-
`tales. Technique & Documentation — Lavoisier, 1995. ISBN: 2-7430-0009-0). Es ware
`jedochvorteilhaft, in héheren Pflanzen, bevorzugt in Olsaaten wie Raps, Lein, Sonnen-
`blume und Soja, LCPUFAsherzustellen, da auf diese Weise grof&e Mengen qualitativ
`hochwertiger LCPUFAsfur die Lebensmittelindustrie, die Tierernahrung und fur
`.
`pharmazeutische Zwecke kostengiinstig gewonnen werden kénnen. Hierzu werden
`vorteilhafterweise Uber gentechnische Methoden Gene,die fir Enzyme der Biosynthe-
`se von LCPUFAskodieren, in Olsaaten eingefiihrt und exprimiert, vorteilhaft im Samen
`exprimiert. Dies sind Gene, die beispielsweise fir A-6-Desaturasen, A-6-Elongasen, A-
`5-Desaturasen, A-5-Elongasen oder A-4-Desaturasen kodieren. Diese Gene kénnen
`vorteilhaft aus Mikroorganismen und niederen Pflanzen isoliert werden, die LCPUFAs
`herstellen und in den Membranen oder Triacylglyceriden einbauen. So konnten bereits
`A-6-Desaturase-Gene aus dem Moos Physcomitrella patens und A-6-Elongase-Gene
`aus P. patens und dem Nematoden C. elegansisoliert werden.
`Fur die Synthese von Arachidonsaure, Eicosapentaensaure (EPA) und Docosahe-
`xaensaure (DHA) werden verschiedene Synthesewegediskutiert (Figur. 1). So erfolgt
`die Produktion von EPA bzw. DHA in marinen Bakterien wie Vibrio sp. oder Shewanel-
`la sp. nach dem Polyketid-Weg (Yu,R.et al. Lipids 35:1061-1064, 2000; Takeyama,H.
`et al. Microbiology 143:2725-2731, 1997).
`
`Ein alternative Strategie verlauft iber die wechseinde Aktivitat von Desaturasen und
`Elongasen (Zank, T.K. et al. Plant Journal 31:255-268, 2002: Sakuradani, E.et al.
`Gene 238:445-453, 1999). Eine Modifikation des beschriebenen WegesUber A6-
`Desaturase, A6-Elongase, A5-Desaturase, A5-Elongase, A4-Desaturase ist der
`Sprecher-Syntheseweg (Sprecher 2000, Biochim. Biophys. Acta 1486:219-231) in
`Saugetieren. Anstelle der A4-Desaturierung erfolgt hier ein weiterer Elongationsschritt
`auf Co4, eine weitere A6-Desaturierung undabschliessend eine B-Oxidation auf die Co2-
`Kettenlange. Fur die Herstellung in Pflanzen und Mikroorganismenist der sogenannte
`Sprecher-Syntheseweg(siehe Figur 1) allerdings nicht geeignet, da die Regulations-
`mechanismen nicht bekannit sind.
`
`Die polyungesattigten Fettsauren kénnen entsprechend ihrem Desaturierungsmusterin
`zwei groke Klassen, in w-6- oder w-3-Fettsauren eingeteiltwerden, die metabolisch
`und funktionell unterschiedlich Aktivitaten haben (Fig. 1).
`
`10
`
`15
`
`20
`
`25
`
`30
`
`35
`
`40
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO2005/083093
`
`PCT/EP2005/001863
`
`7
`
`Als Ausgangsproduktfiir den w-6-Stoffwechselweg fungiert die Fettsaure Linolsaure
`(18:2°°:'?), wahrend der w-3-Weg Uber Linolensaure (18:34°'?*) ablauft. Linolensaure
`wird dabei durch Aktivitat einer w-3-Desaturase gebildet (Tocheret al. 1998, Prog.
`Lipid Res. 37, 73-117 ; Domergueet al. 2002, Eur. J. Biochem. 269, 4105-4113).
`
`Saugetiere und damit auch der Mensch verftigen Uber keine entsprechende Desaiura-
`seaktivitat (A-12- und w-3-Desaturase) und missen diese Fettsauren (essentielle
`Fettsauren) tiber die Nahrung aufnehmen. Uber die Abfolge von Desaturase- und
`Elongase-Reaktionen werden dann aus diesen Vorstufen die physiologisch wichtigen
`polyungesattigten Fetts4uren Arachidonsaure (= ARA, 20:44°°:"""4) eine w-6-Fettsaure
`und die beiden w-3-Fettsauren Eicosapentaen- (= EPA, 20:5°°%"""4-'7) und Docosahe-
`xaensaure (DHA, 22:644719'9:17-'9) synthetisiert. Die Applikation von w-3-Fettsauren
`zeigt dabei die wie oben beschrieben therapeutische Wirkung bei der Behandlung von
`Herz-Kreislaufkrankheiten (Shimikawa 2001, World Rev. Nutr. Diet. 88, 100-108),
`Entziindungen (Calder 2002, Proc. Nutr. Soc. 61, 345-358) und Arthridis (Cleland und
`James 2000,J. Rheumatol. 27, 2305-2307).
`
`Aus ernahrungsphysiologischer Sicht ist es deshalb giinstig eine Verschiebung
`zwischen dem w-6-Syntheseweg und dem w-3-Syntheseweg(siehe Figur1) zu
`erreichen, so dass mehr w-3-Fettsauren hergestellt werden. In der Literatur wurden die
`enzymatischen Aktivitaten verschiedener w-3-Desaturasen beschrieben,die Cyg:2-,
`Czo.4- Oder Cz2-5-Fettsauren desaturieren (siehe Figur 1). Keine der biochemisch-
`beschriebenen Desaturasen setzt jedoch ein breites Substratspektrum des w-6-
`_ Synthesewegs zu den entsprechenden Fettsauren des w-3-Syntheseweg um.
`
`Die Verlangerung von Fettsauren durch Elongasen um 2 bzw. 4 C-Atomeist fur die
`Produktion von C29- bzw. C22-PUFAs von entscheidender Bedeutung. Dieser Prozess
`verlauft Uber 4 Stufen. Der erste Schritt stellt die Kondensation von Malonyl-CoA an
`das Fettsaure-Acyl-CoA durch die Ketoacyl-CoA-Synthase (KCS,im weiteren Text als
`Elongase bezeichnet). Es folgt dann ein Reduktionschritt (Ketoacyl-CoA-Reduktase,
`KCR), ein Dehydratationsschritt (Dehydratase) und ein abschliessender Reduktions-
`schritt (enoyl-CoA-Reduktase). Es wurde postuliert, dass die Aktivitat der Elongase
`die Spezifitat und Geschwindigkeit des gesamten Prozesses beeinflussen (Millar and
`Kunst, 1997 Plant Journal 12:121-131).
`
`Zur Herstellung von DHA (C22:6 n-3) in Organismen, die diese Fettsdure nattirlicher-
`weise nicht produzieren, wurde bisher keine spezifische Elongase beschrieben. Bisher
`wurden nur Elongasen beschrieben, die C2p- bzw. Co4-Fettsauren bereitstellen. Eine A-
`5-Elongase-Aktivitat wurde bisher noch nicht beschrieben.
`
`Erste transgene Pflanzen, die fur Enzyme der LCPUFA-Biosynthese kodierende Gene
`enthalten und exprimieren und als Folge dessen LCPUFAsproduzieren, wurden
`beispielsweise in DE 102 19 203 (Verfahren zur Herstellung mehrfach ungesattigter
`Fettsauren in Pflanzen) oder WO 2004/071467 beschrieben. Diese Pflanzen produzie-
`ren allerdings LCPUFAs in Mengen, die fiir eine Aufarbeitung der in den Pflanzen
`enthaltenen Ole noch weiter optimiert werden missen. So betragt der Gehalt von ARA
`
`10
`
`15
`
`20
`
`25
`
`30
`
`35
`
`40
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO2005/083093
`
`PCT/EP2005/001863
`
`,
`
`8
`
`in den in DE-A-102 19 203 beschriebenen Pflanzenlediglich 0,4 bis 2% und der Gehalt
`von EPAlediglich 0,5 bis 1%, jeweils bezogen auf den Gesamtlipidgehalt der Pflanze.
`In WO 2004/071467 werden héhere Gehalte an mehrfach ungesattigten Cao- und Cz2-
`Fettsauren, wie ARA, EPA oder DHA offenbart. Jedoch.weist das offenbarte Verfahren
`einige gravierende Nachteile auf. DHAlasst sich im offenbarten Verfahren offenbar
`berhauptnicht im Samen nachweisen. Fureine Herstellung von PUFAs ist Soja
`aufgrund des geringen Olgehalts von ca. nur 20 Gew.-% weniger geeignet. Sojaist
`eine vorteilhafte Proteinquelle und wird deshalb in groRem Umfang angebaut. Der
`Olgehalt von Soja ist jedoch eher gering. Weiterhin ist der im Herstellungsverfahren
`erzielte Gehalt an Dihomo-y-linolensaure (=DGHL oder HGLA)viel zu hoch. In Fisch-
`oder Algendlen oder mikrobiellen Olen ist HGLA kaum nachweisbar. Ein weiterer
`Nachteil ist, dass die in WO 2004/071467 offenbarten Pflanzen durch Cotransformation
`erzeugt wurden,diesfuhrt zur Aufspaltung der Eige