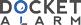`PATENTWESENS (PCT) VEROFFENTLICHTE INTERNATIONALE ANMELDUNG
`
`(19) Weltorganisation fiir geistiges Eigentum
`Internationales Buro
`
`9. September 2005 (09.09.2005)
`
`(43) Internationales Veroffentlichungsdatum
`
`(10) Internationale Veroffentlichungsnummer
`
`WO 2005/083093 A2
`
`(51) Internationale Patentklassifikation7:
`_
`_
`(21) Internatlonales Aktenzelchen:
`(22) Internationales Anmeldedatum:
`23. Februar 2005 (23.02.2005)
`
`PCT/EP2005/001863
`
`C12N 15/82
`
`(25) Einreichungssprache:
`
`(26) Veroffentlichungssprache:
`(30) Angaben zur Prioritat:
`10 2004 009 457.8
`
`Deutsch
`
`Deutsch
`
`27. Februar 2004 (27.02.2004)
`
`DE
`
`10 2004 012 370.5
`10 2004 017 518.7
`10 2004 024 014.0
`PCT/EP/04/07957
`10 2004 062 543-3
`24. Dezember 2004 (24.12.2004) DE
`
`13. Marl 2004 (13.03.2004) DE
`8. April 2004 (08.04.2004) DE
`14. Mai 2004 (14.05.2004) DE
`16. Juli 2004 (16.07.2004)
`EP
`
`(71) Anmelder (fiir alle Bestimmungsstaaten mitAusnahme von
`US): BASF PLANT SCIENCE GmbH [DE/DE]; 67056
`L d '
`h f DE.
`u ngs a en (
`)
`(72) Erfinder; und
`(75) Erfinder/Anmelder
`
`(nur fiir US): CIRPUS, Petra
`
`[Fortsetzung auf der na'chsten Seite]
`
`(54) Title: METHOD FOR PRODUCING POLYUNSATURATED FATTY ACIDS IN TRANSGENIC PLANTS
`
`(54) Bezeichnung: VERFAHREN ZUR HERSTELLUNG MEHRFACH UNGESATTIGTER FETTSAUREN IN TRANSGENEN
`PFLANZEN
`
`11
`Velschledenn Symnwaege zur Elosynthese Von DHA (Dmahexaensnuue)
`
`B
`
`ms-
`ma.
`athwa
`a wa
`
`
`
`
`yfimsmse M y
`p
`49.9mm.“ /1a2\: A—qmsmse;24< ”Elam”
`2mm 1mm“
`1824.42.15
`203......”
`48'”’”"'"’3“~‘\ / ‘5*’°"9"‘5\ / 424mm,...
`ZOTAWM ‘
`”TM?
`
`FF C
`mm“
`20.545.41.47
`
`
`
`:13:-
`457.1029...
`’1'“
`5""
`..
`._
`i
`7
`,__.
`
`*giadesagme
`Emmmezms H M
`l
`A4-desaturase
`l
`A541
`f
`22.5 mama fizzfimlwnuws ._ ;
`-
`.
`, 1'
`24646912154
`Nassau...” m WW"
`
`
`
`A
`“‘5
`“EM-W
`MalonyI-CoA
`
`(57) Abstract: The invention relates to a method for producing
`.
`.
`.
`.
`polyunsaturated fatty ac1ds 1n seeds of transgenic plants. According
`g
`P YP P
`to said method, nucleic acids, codin
`for
`01
`e tides with a
`(o—3—desaturase, A—l2—desaturase, A—6—desaturase, A—6—elongase,
`A—5—desaturase, A—5—elongase and/or A—4—desaturase
`activity,
`preferably for polypeptides with a A—6—desaturase, A—6—elongase
`and A—5—desaturase activity, are introduced into the organism. The
`nucleic acid sequences are represented by SEQ ID NO: 11, SEQ ID
`NO: 27, SEQ ID NO: 193, SEQ ID NO: 197, SEQ ID NO: 199 and
`SEQ ID NO: 201. Advantageously, said nucleic acid sequences can
`be ex ressed in the or anism o tionall
`to ether with other nucleic
`P
`g
`P
`y
`g
`acid se uences that code for
`01
`e tides of the bios nthesis
`q
`p yp p
`y
`of the fatty acid or lipid metabolism. Nucleic acid sequences
`coding for a A—6—desaturase, A—5—desaturase, A—4—desaturase,
`A—l 2—desaturase and/or A—6—elon ase activit
`are es eciall
`g
`y
`P
`y
`.
`.
`.
`.
`.
`-
`advantageous. Advantageously, said desaturases and elongases
`originate from thalasswsna, euglena or ostreococcus. The invention
`also relates to a method for producing oils and/or triacylglycerides with an increased content of long—chain polyunsaturated fatty
`acids. In a preferred embodiment, the invention also relates to a method for producing arachidonic acid, eicosapentaenic acid or
`docosahexaenic acid, and to a method for producing triglycerides with an increased content of unsaturated fatty acids, especially
`arachidonic acid, eicosapentaenoic acid and/or docosahexaenoic acid, in transgenic plants, preferably in seeds of the transgenic
`plants. The invention further relates to the production of a transgenic plant with an increased content of polyunsaturated fatty acids,
`especially arachidonic acid, eicosapentaenoic acid and/or docosahexaenoic acid, based on the expression of the elongases and
`desaturases used in the inventive method. The invention also relates to recombinant nucleic acids molecules containing, together
`or individually, nucleic acid sequences coding for the polypeptides with a A—6—desaturase, A—6—elongase, A—5—desaturase and
`
`.
`mwm,
`22.3.2.0...”
`
`FF
`SPEAKER PATHWAY
`11...VARIOUSSYNTHESE-WAYFORBIOSYNTHESEOF DHA(ACIDDOCOSAHEXAENOIC)
`
`
`
`93A2|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
`
`c A—5—elongase activity, and transgenic plants containing said recombinant nucleic acid molecules. Another part of the invention
`m relates to oils, lipids and/or fatty acids produced according to the inventive method, and to the use thereof. Furthermore, the
`w invention relates to unsaturated fatty acids and triglycerides with an increased content of unsaturated fatty acids, and to the use of
`E the same.
`
`(57) Zusammenfassung: Die vorliegende Erfindung betrifft ein Verfahren zur Herstellung von mehrfach ungesattigten Fettsauren
`0
`N im Samen transgener Pflanzen, indem Nukleinsauren in den Organismus eingebracht werden, die fur Polypeptide mit (o—3—Desa—
`turase—, A—l2—Desaturase—, A—6—Desaturase—, A—6—Elongase—, A—5—Desaturase—, A—5—Elongase— und/oder A—4—Desaturaseaktivitat
`O bevorzugt fur Polypeptide mit A—6—Desaturase—,
`a
`
`[Fortsetzung aufder na'chsten Seite]
`
`5 c
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO 2005/083093 A2
`
`|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
`
`[DE/DE];Landtei1str.12, 68163 Mannheim (DE). BAUER,
`Jorg [DE/DE]; Thorwaldsenstr. 1A, 67061 Ludwigshafen
`(DE). QIU, Xiao [CA/CA]; 403 Kendardine Road, Saska—
`toon Sk. S7N 335 (CA). WU, Guohai [CA/CA]; 2103
`Kenderdine Road, Saskatoon Sk. S7N 4A9 (CA). DATLA,
`Nagamani [CA/CA]; 527 Bayview Terrace, Saskatoon Sk.
`S7V 1B6 (CA),
`
`c/o BASF Aktienge—
`PRESSLER, Uwe;
`(74) Anwalt:
`sellschaft, 67056 Ludwigshafen (DE).
`
`TM, TN, TR, TT, TZ, UA, UG, US, UZ, VC, VN, YU, ZA,
`ZM, ZW.
`
`(84) Bestimmungsstaaten (soweit nicht anders angegeben, fiir
`jede verffigbare regionale Schutzrechtsartfi ARIPO (BW,
`GH, GM, KE, LS, MW, MZ, NA, SD, SL, SZ, TZ, UG,
`ZM, ZW), eurasisches (AM, AZ, BY, KG, KZ, MD, RU,
`TJ, TM), europ'aisches (AT, BE, BG, CH, CY, CZ, DE, DK,
`EE, ES, FI, FR, GB, GR, HU, IE, IS, IT, LT, LU, MC, NL,
`PL, PT, RO, SE, SI, SK, TR), OAPI (BF, BJ, CF, CG, CI,
`CM, GA, GN, GQ, GW, ML, MR, NE, SN, TD, TG).
`
`(81) Bestimmungsstaaten (soweit nicht anders angegeben, fiir Veroffentlicht:
`jade verfligbare nationale Schutzrechlsdfi): AE, AG, AL, — ohne internationalen Recherchenbericht und emeut zu ver—
`AM, AT, AU, AZ, BA, BB, BG, BR, BW, BY, BZ, CA, CH,
`bffentlichen nach Erhalt des Berichts
`CN, CO, CR, CU, CZ, DE, DK, DM, DZ, EC, EE, EG, ES,
`FI, GB, GD, GE, GH, GM, HR, HU, ID, IL, IN, IS, JP, KE,
`KG, KP, KR, KZ, LC, LK, LR, LS, LT, LU, LV, MA, MD,
`MG, MK, MN, MW, MX, MZ, NA, NI, NO, NZ, OM, PG,
`PH, PL, PT, RO, RU, SC, SD, SE, SG, SK, SL, SM, SY, TJ,
`
`Zur Erkla'rung der Zweibuchstaben— Codes und der anderen Ab—
`kiirzungen wird auf die Erkla‘rungen ( ”Guidance Notes on C0—
`des and Abbreviations ”) am Anfangjeder reguldren Ausgabe der
`PCT—Gazette verwiesen.
`
`A—6—Elongase— und A—S—Desaturaseaktivit'at codieren. Bei den Nukleinsauresequenzen handelt es sich um die in SEQ ID NO: 11,
`SEQ ID NO: 27, SEQ ID NO: 193, SEQ ID NO: 197, SEQ ID NO: 199 und SEQ ID NO: 201 dargestellten Sequenzen. Vorteil—
`haft konnen diese Nukleinsauresequenzen gegebenenfalls zusammen mit weiteren Nukleinsauresequenzen, die fiir Polypeptide der
`Biosynthese des Fettsaure— oder Lipidstoffwechels codieren, in dem Organismus exprimiert werden. Besonders vorteilhaft sind Nuk—
`leinsauresequenzen, die fiir eine A—6—Desaturase—, eine A—S—Desaturase—, A—4—Desaturase—, A—1 2—Desaturase— und/oder A—6—Elon—
`gaseaktivitat codieren. Vorteilhaft stammen diese Desaturasen und Elongasen aus Thalassiosira, Euglena oder Ostreococcus. Weiter—
`hin betrifft die Erfindung ein Verfahren zur Herstellung von Qlen und/oder Triacylglyceriden mit einem erhohten Gehalt an langket—
`tigen mehrfach ungesattigten Fettsauren. Die Erfindung betrifft in einer bevorzugten Ausfiihrungsforrn ausserdem ein Verfahren zur
`Herstellung von Arachidonsaure, Eicosapentaensaure oder Docosahexaensaure sowie ein Verfahren zur Herstellung von Triglyceri—
`den mit einem erhohten Gehalt an ungesattigten Fettsauren, insbesondere Arachidonsaure, Eicosapentaensaure und/oder Docosa—
`hexaensaure, in transgenen Pflanzen vorteilhaft im Samen der transgenen Pflanze. Die Erfindung betrifft die Herstellung einer
`transgenen Pflanze mit erhohtem Gehalt an mehrfach ungesattigten Fettsauren, insbesondere Arachidonsaure, Eicosapentaensaure
`und/oder Docosahexaensaure, aufgrund der Expression der im erfindungsgemassen Verfahren verwendeten Elongasen und Desat—
`urasen. Die Erfindung betrifft weiterhin rekombinante Nukleinsauremolekiile, die die Nukleinsauresequenzen, die fiir die Polypep—
`tide mit A—6—Desaturase—, A—6—Elongase—, A—S —Desaturase— und A—S —Elongaseaktivitat kodieren, gemeinsam oder einzeln enthalten,
`sowie transgene Pflanzen, die die vorgenannten rekombinanten Nukleinsauremolekiile enthalten. Ein weiterer Teil der Erfindung
`betrifft Qle, Lipide und/oder Fettsauren hergestellt nach dem erfindungsgemassen Verfahren und deren Verwendung. Ausserdem
`betrifft die Erfindung ungesattigte Fettsauren sowie Triglyceride mit einem erhohten Gehalt an ungesattigten Fettsauren und deren
`Verwendung.
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO 2005/083093
`
`‘
`
`PCT/EP2005/001863
`
`Verfahren zur Herstellung mehrfach ungeséittigter Fettséuren in transgenen
`Pflanzen
`
`Beschreibung‘
`
`Die vorliegende Erfindung betrif'ft ein Verfahren zur Herstellung von mehrfach unge-
`‘séttigten Fettséiuren im Samen transgener Pflanzen, indem Nukleinséuren in den
`Organismus eingebracht werden, die fiir Polypeptide mit w-3-Desaturase—, A—12—
`Desaturase-, A—6-Desaturase-, A-6-EIongase—, A—5-Desaturase-, A-5-Elongase-
`und/oder A—4-Desaturaseaktivitéit bevorzugt fiJr Polypeptide mit A—B-Desaturase—, A—6-
`
`Elongase- und A—5-Desaturaseaktivitét codieren.
`
`10
`
`15
`
`Bei den Nukleinséiuresequenzen handelt es sich um die in SEQ ID NO: 11, SEQ ID
`NO: 27, SEQ ID NO: 193, SEQ ID NO: 197, SEQ ID NO: 199 und SEQ ID NO: 201
`dargestellten Sequenzen. Bevorzugt wird neben diesen Nukleinséuresequenzen eine
`weitere Nukleinséuresequenz, die f'Lir ein Polypeptid mit einer A—12-Desaturaeeaktivitét
`kodiert, in die Pflanze eingebracht und ebenfalls gleichzeitig exprimiert. Besonders
`bevorzugt handelt es sich dabei um die in SEQ ID NO: 195 dargestellte Nukleinséure—
`sequenz.
`
`20'
`
`25
`
`30
`
`35
`
`Vorteilhaft kénnen diese Nukleinséiuresequenzen gegebenenfalls zusammen mit
`weiteren Nukleinséuresequenzen, die fiir Polypeptide der Biosynthese des Fettséiure-
`oder Lipidstoffwechels codieren, in dem Organismus exprimiert werden. Besonders
`vorteilhaft sind Nukleinséuresequenzen, die fiJreine A-6—Desaturase—, eine'A-5-
`Desaturase-, A—4—DesatLirase-, A—12—Desaturase— und/oder A—6-Elongaseaktivitét
`codieren. Vorteilhaft stammen diese Desaturasen und_ Elongasen aus Thalassiosira,
`Euglena oder Ostreococcus. Weiterhin betrifft die Erfindung ein Verfahren zur Herstel4 '
`lung von Olen und/oder Triacylglyceriden mit einem er'hohten Gehalt an Iangkettigen
`mehrfach ungeséttigten Fettséiuren.
`'
`
`.
`
`Die Erfindung betrlfft in einer bevorzugten Ausfflhrungsform auBerdem ein Verfahren
`zur Herstellung von Arachidonséiure, Eicosapentaenséure oder Docosahexaenséiure
`sowie ein Verfahren zur Herstellung von Triglyceriden mit einem erhdhten Gehalt an
`ungeséittigten Fettséuren, insbesondere Arachidonséure, Eicosapentaenséure
`und/oder Docosahexaenséure, in transgenen Pflanzen vorteilhaft im Samen der’
`transgenen Pflanze. Die Erfindung betrifft die Herstellung einer transgenen Pflanze mit
`erhéhtem Gehalt an mehrfach ungeséttigten Fettséiuren, insbesondere Araohidonséu-
`re, Eicosapentaenséure und/oder Docosahexaenséure, aufgrund der Expression der
`im erfindungsgeméBen Verfahren verwendeten Elongasen und Desaturasen.
`
`Die Erfindung betrifft weiterhin rekombinante Nukleinséuremolekule, die die Nuklein-
`séiuresequenzen, die fUr die Polypeptide mit A—6—Desaturase-, A—G—EIongase-, A—5-
`Desaturase— und A-5-Elongaseaktivitét kodieren, gemeinsam oder einzeln enthalten,
`sowie transgene Pflanzen, die die vorgenannten rekombinanten Nukleinséuremolekiile
`enthalten.
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO 2005/083093
`
`PCT/EP2005/001863
`
`2
`
`Ein weiterer Teil der Erfindung betrifft Ole, Lipide und/oder Fettsauren hergestellt
`nach dem erflndungsgemalzen Verfahren und deren Ventvendung. AulSerdem betrifft
`die Erfindung ungesattigte Fettsauren sowie Triglyceride mit einem erhohten Gehalt an
`ungesattigten Fettsauren und deren Venn/endung.
`
`Die Lipidsynthese lasst sich in zwei Abschnitte unterteilen: die Synthese von Fettsau—
`ren und ihre Bindung an sn-Glycerin-B—Phosphat sowie die Addition oder Modifikation
`einer polaren Kopfgruppe. Ubliche Lipide, die in Membranen venNendet werden,
`umfassen Phospholipide, Glycolipide, Sphingolipide und Phosphoglyceride. Die
`Fettsauresynthese beginnt mit der Umwandlung von Acetyl-CoA in Malonyl-CoA durch
`die Acetyl-CoA-Carboxylase oder in Acetyl-ACP durch die Acetyltransacylase. Nach
`einer Kondensationsreaktion bilden diese beiden Produktmolekule Zusammen Aceto-
`acetyl-ACP, das Uber eine Reihe von Kondensations-, Reduktions- und Dehydratisie-
`rungsreaktionen umgewandelt wird, so dass ein gesattigtes Fettsauremolekfll mit der
`gewiinschten Kettenlange erhalten wird. Die Produktion der ungesattigten Fettsauren
`aus diesen Molekulen wird durch spezifische Desaturasen katalysiert, und zwar
`entweder aerob mittels molekularem Sauerstoff oder anaerob (bezflglich der Fett-
`V sauresynthese in Mikroorganismen siehe F.C. Neidhardt et al. (1996) E. coli und
`Salmonella. ASM Press: Washington, D.C., S. 612-636 und darin enthaltene Literatur-
`stellen; Lengeler et al. (Hrsgb.) (1999) Biology of Procaryotes. Thieme: Stuttgart, New
`York, und die enthaltene Literaturstellen, sowie Magnuson, K., et al. (1993) Microbiolo-
`gical Reviews 57:522-542 und die enthaltenen Literaturstellen). Die so hergestellten an
`Phospholipide gebundenen Fettsauren mUssen anschlieBend filr die weiteren Elonga-
`tionen aus den Phospholipiden wieder in den FettsaureCoA-Ester-Pool UberfiJhrt
`werden. Dies ermoglichen Acyl-CoA:Lysophospholipid-Acyltransferasen. Weiterhin
`konnen diese Enzyme die elongierten Fettsauren wieder von den CoA—Estern auf die
`Phospholipide Ubertragen. Diese Reaktionsabfolge kann gegebenenfalls mehrfabh
`durchlaufen werden.
`
`.
`
`Ferner mlesen Fettsauren anschliersend an verschiedene Modifikationsorte transpor-
`
`tiert und in das Triacylglycerin—Speicherlipid eingebaut werden. Ein weiterer wichtiger
`Schritt bei der Lipidsynthese ist der Transfer von Fettsauren auf die polaren Kopf—
`gruppen, beispielsweise durch Glycerin-Fettsaure—Acyltransferase (siehe Frentzen,
`1998, Lipid, 100(4-5):161-166).
`
`Veroffentlichungen fiber die Pflanzen-Fettsaurebiosynthese, Desaturierung, den Lipid-
`stoffwechsel und Membrantransport von fetthaltigen Verbindungen, die Betaoxidation,
`Fettsauremodifikation und Cofaktoren, Triacylglycerin-Speicherung und -
`Assemblierung einschliel'slich der Literaturstellen darin siehe in den folgenden Artikeln:
`Kinney, 1997, Genetic Engeneering, Hrsgb.: JK Setlow, 19:149-166; Ohlrogge und
`Browse, 1995, Plant Cell 7:957-970; Shanklin und Cahoon, 1998, Annu. Rev. Plant
`Physiol. Plant Mol. Biol. 49:611-641; Voelker, 1996, Genetic Engeneering, Hrsgb.: JK
`Setlow, 18:111—13; Gerhardt, 1992, Prog. Lipid R. 31:397-417; GUhnemann-Schafer &
`Kindl, 1995, Biochim. Biophys Acta 1256:181-186; Kunau et al., 1995, Prog. Lipid Res.
`34:267—342; Stymne et al., 1993, in: Biochemistry and Molecular Biology of Membrane
`
`10
`
`15'
`
`20
`
`25
`
`30
`
`35
`
`40
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO 2005/083093
`
`PCT/EP2005/001863
`
`3
`
`and Storage Lipids of Plants, Hrsgb.: Murata und Somerville, Rockville, American
`Society of Plant Physiologists, 150-158, Murphy & Ross 1998, Plant Journal. 13(1):1-
`16.
`
`lm folgendenlwerd'en mehrfach ungesattigte' Fettsauren als PUFA, PUFAs, LCPUFA
`oder LCPUFAs bezeichnet (p_oly gnsaturated fatty _a_cids, PUFA, mehrfach ungesattigte
`Fettsauren;_long _c_hain goly gnsaturated fatty acids, LCPUFA, Iangkettige mehrfach
`ungesattigte Fettsauren).
`'
`
`Fettsauren und Triacylglyceride haben eine Vielzahl von Anwendungen in der
`Lebensmittelindustrie, der Tierernahrung, der Kosmetik und im Pharmabereioh.
`Je nachdem, ob es sich um freie gesattigte und ungesattigte Fettsauren‘oder um
`- Triacylglyceride mit einem erhohten Gehalt an geséittigten oder-ungesattigten Fett-
`sauren handelt, 'sind sie f'L'lr die unterschiedlichsten Anwendungen geeignet. Mehrfach-
`ungesattigte Fettsauren wie Linol- und Linolensaure sind fiJr Séugetiere essentiell,
`da sie nicht von diesen selbst hergestellt werden konnen. Deshalb stellen mehrfach
`ungeséittigte w-3-Fettsauren und w-G—Fettsauren einen wichtigen Bestandteil der
`tierischen und menschlichen Nahrung dar. So werden z.B. in der humanen Ernahrung
`Lipide mit ungesattigten Fettsauren, speziell mehrfach ungesattigten, Fettsauren
`bevorzugt. Den mehrfach ungesattigten w-3-Fettsauren wird dabei ein positiver Effekt
`auf den Cholesterinspiegel im Blut und damit auf die Pravention einer Herzerkrankung
`zugeschrieben. Durch Zugabe dieser w-3-Fettsauren zur Nahrung kann das Risiko
`,einer Herzerkrankung, eines Schlaganfalls oder von Bluthochdruck deutlich verringert
`werden (Shimikawa 2001, World Rev. Nutr. Diet. 88, 100-108).
`
`Auch entztindliche, speziell chronisch entzflndliche, Prozesse im Rahmen immunologi-
`scher Erkrankungen wie rheumatoider Arthritis lassen sich durch w-3-Fettsauren
`positiv beeinflussen (Calder 2002, Proc. Nutr. Soc. 61, 345—358; Cleland und James
`2000, J. Rheumatol. 27, 2305-2307). Sie werden deshalb Lebensmitteln, speziell
`diatetischen Lebensmitteln, zugegeben oder finden in Medikamenten Anwendung. 03-6-
`Fettsauren wie Arachidonsaure Uben bei diesen rheumatischen Erkrankungen eher
`
`einen negativen Effekt aus.
`
`w-3— und w-6—Fettsauren sind Vorlaufer von Gewebshormonen, den sogenannten
`Eicosanoiden wie den Prostaglandinen, die sich von der Dihomo-v—linolensaure,
`der Arachidonsaure und der Eicosapentaenséiure ableiten, und den Thromboxanen
`und Leukotrienen, die sich von der Arachidons'a'ure und der Eicosapentaensaiure
`ableiten. Eicosanoide (sog. PGz-Serie), die aus w-6-Fetts'a'uren gebildet werden,
`fordern in der Regel Entztindungsreaktionen, wahrend Eicosanoide (sog. PGs-Serie)
`aus w-3-Fettsauren geringe oder keine entzflndungsfordernde Wirkung haben.
`
`Mehrfach ungesattigte langkettige w-3-Fettsauren wie Eicosapentaensaure (= EPA,
`C2025A5'8'11'14'17) oder Docosahexaensaure (= DHA, 022:6A4'7'1°'13'16'19) sind wichtige
`Komponenten der menschlichen Ernahrung aufgrund ihrer verschiedenen Rollen in der
`Gesundheit, die Aspekte wie die Entwicklung des kindlichen Gehirns, der Funktionalitat
`des Auges, der Synthese von Hormonen und anderer Signalstoffe, sowie die Vorbeu—
`
`10'
`
`15
`
`20
`
`25
`
`3'0
`
`35
`
`40
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`' WO 2005/083093
`
`PCT/EP2005/001863
`
`4
`
`gung von Herz-Kreislauf-Beschwerden, Krebs und Diabetes umfassen (Pouios, A
`Lipids 30:1-14, 1995; Horrocks, LA und Yeo YK Pharmacol Res 40:211-225, 1999). Es
`besteht aus diesem Grund ein Bedari an der Produktion mehrfach ungeSattigter
`
`Iangkettiger Fetts'a‘uren.
`
`Aufgrund der heute i'Iblichen Zusammensetzung der menschlichen Nahrung ist ein
`Zusatz von mehrfach ungesattigten w-3-Fettsauren, die bevorzugt in Fischc‘jlen
`vorkommen, zur Nahrung besonders wichtig. So werden beisbielsweise mehrfach
`ungesattigte Fettsauren wie Docosahexaensa‘ure (= DHA, C22: 6A4W71°131619) oder
`Eisosapentaensa‘ure (= EPA C20: 5As811 1417) Babynahrung zur Erhbhung des
`Na'hrwertes zugesetzt Der ungesattigten Fettsaure DHA wird dabei ein positiver Effekt
`auf die Entwicklung und Aufrechterhaltung von Gehirnfunktionen zugeschrieben. Es
`besteht aus diesem Grund ein Bedarf an der Produktion mehrfach ungeséttigter
`
`langkettiger Fettsaiuren.‘
`
`-
`
`HaL‘Iptsachlich werden die verschiedenen Fettsauren und Triglyceride aus Mikro-
`organismen wie Mortierella oder Schizochytrium oder aus Oi—produzierenden Pflanzen
`wie Soja, Raps, Algen wie Crypthecodinium oder Phaeodactyium und weiteren ge—
`wonnen, wobei sie in der RegelIn Form ihrer Triacylglyceride (= Triglyceride= Tri-
`glycerole) anfallen. Sie kbnnen aber auch aus Tieren wie z. B. Fischen gewonnen
`werden. Die freien Fettsa'uren werden vorteilhaft durch Verseifung hergestellt. Sehr
`_|angkettige mehrfach ungesattigte Fettsauren wie DHA, EPA, Arachidonsaure (= ARA,
`020:4A5'8'11'1‘1), .Dihomo-y—linolensaure (620:3A3'11'1‘1) oder Docosapentaensaure (DPA,
`022:5‘17'1‘1'13'111'19) werden in Olfruchtpfianzen wie Raps, .Soja, Sonnenbiume, Farber-
`saflor nicht synthetisiert. Ubliche natiJrliche Quellen fiJr diese Fettsauren sind Fische
`wie Hering, Lachs, Sardine, Goldbarsch, Aal, Karpfen, Forelle, Heilbutt, Makrele,
`Zander oder Thunfisch oder Algen.
`
`Je nach Anwendungszweck werden ("Die mit gesattigten oder ungeséittigten Fettséuren
`bevorzugt. So werden 2.8. in der humanen Ernahrung Lipide mit ungesattigten Fett—
`sauren spezieil mehrfach ungesattigten Fettsauren bevorzugt. Den mehrfach unge-
`sattigten w-B-Fettsauren wird dabei ein positiver Effekt auf den Cholesterinspiegel
`im Blut und damit auf die Mbglichkeit der Pravention einer Herzerkrankung zuge-
`schrieben. Durch Zugabe dieser wLS-Fettsauren zur Nahrung kann das Risiko einer
`Herzerkrankung, eines Schlaganfalls oder von Bluthocher'Ick deutlich verringert
`werden. Auch entziJndliche spezieil chronisch entzi'Indliche Prozesse im Rahmen
`immunologischer Erkrankungen wie rheumatroider Arthritis Iassen sich durch w-3-
`Fettsauren positiv beeinflussen. Sie werden deshalb Lebensmitteln spezieil diatischen
`Lebensmitteln zugegeben oder finden in Medikamenten Anwendung. w-B—Fettséuren
`wie Arachidonséure haben bei diesen rheumatischen Erkrankungen aufgrund unserer
`inIichen Nahrungsmittelzusammensetzung eher einen negativen Effekt auf diese
`Krankheiten.
`
`10
`
`15
`
`20
`
`'25
`
`3O
`
`35
`
`4O
`
`Aufgrund ihrer pbsitiven Eigenschaften hat es in der Vergangenheit nicht an Ansatzen
`gefehit, Gene, die an der Synthese von Fettsauren bzw. Triglyceriden beteiligt sind, f'L'Ir
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO 2005/083093
`
`PCT/EP2005/001863
`
`5
`
`die Herstellung von Olen in verschiedenen Organismen mit geandertem Gehalt' an
`ungeséttigten Fettsauren verfiigbar zu machen. So wird in WO 91/13972 und seinem
`US—Aquivalent eine A—9-Desaturase beschrieben. In WO 93/11245 wird eine A—15—
`Desaturase in WO 94/11516 wird eine A—12—Desaturase beansprucht. Weitere
`Desaturasen Werden beispielsweise in EP—A—0 550 162, WO 94/18337, WO 97/30582,
`WO 97/21340, WO 95/18222, EP—A—0 794 250, Stukey et al., J. Biol. Chem. 265,
`1990: 20144—20149, Wada et al., Nature 347,19902200—203 oder Huang et al., Lipids
`34,1999:649—659 beschrieben. Die biochemische Charakterisierung der verschie-
`denen Desaturasen ist jedoch bisher nur unzureichend erfolgt, da die Enzyme als
`membrangebundene Proteine nur sehr schwer zu isolieren und zu charakterisieren
`sind (McKeon et al., Methods'In Enzymol.71, 1981: 12141—12147,Wang et aL, Plant
`Physiol. Biochem.,26, 1988. 777—792). In der Regel erfolgt die Charakterisierung
`membrangebundener Desaturasen durch Einbringung in einen geeigneten Organis-
`xmus, der anschlieiSend auf Enzymaktivit'a‘t mittels Edukt- und Produktanalyse unter-
`sucht wird. A—6—Desaturasen werden in WO 93/06712, US 5,614,393, US5614393,
`WO 96/21022, W000/21557 und WO 99/27111 beschrieben. Die Anwendung zur
`Produktion in transgenen Organismen wird in W098/46763 W098/46764, W09846765
`beschrieben. Die Expression verschiedener Desaturasen wird in W099/64616 oder
`W098/46776 beschrieben und beansprucht. Bzgl. der Effektivitat der Expression von
`Desaturasen und ihrem Einfluss auf die Bildung mehrfach ungesattigterFettsauren ist
`anzumerken dass durch Expression einer einzelnen Desaturase wie bisher beschrie-
`. ben Iediglich geringe Gehalte an ungeséttigten Fettsauren/Lipiden wie z. B. y-
`Linolenséiure und Stearidonsaure erreicht wurden.
`
`In der Vergangenheit wurden zahIreiche Versuche unternommen, EIongase-Gene
`zu erhalten. Millar and Kunst, 1997 (Plant Journal 12: 121- 131) und Millar et aL, 1999
`(Plant Cell 11:825-838) beschreiben die Charakterisierung von pflanzlichen Elongasen
`zur Synthese von einfach ungesattigten Iangkettigen Fettsauren (C22: 1) bzw. zur
`Synthese von sehr Iangkettigen Fetts'a‘uren fL'Ir die Wachsbildung in Pflanzen (Cm-Caz).
`Beschreibungen zur synthese von Arachidonsaure und EPA finden sich beispielsweise
`in WO 01/59128, WO 00/12720, WO 02/077213 und WO 02/08401. Die Synthese von
`mehrfach ungesattigter C24-Fettsauren ist beispielsweise in Tvrdik et al. 2000, J. Cell
`~ Biol. 149:707-718 oder WO 02/44320 beschrieben.
`
`Besonders geeignete Mikroorganismen zur Herstellung von PUFAs sind Mikro—
`organismen wie Mikroalgen wie Phaeodactylum tricornutum, Porphiridium-Arten,
`Thraustochytrien—Arten, Schizochytrien-Arten ocler Crypthecodinium—Arten, Ciliaten,
`wie Stylonychia oder Colpidium, PiIze, wie Mortierella, Entomophthora oder Mucor
`und/oder Moosen wie Physcomitrella, Ceratodon und Marchantia (R. Vazhappilly & F.
`Chen (1998) Botanica Marina 41: 553-558; K. Totani & K. Oba (1987) Lipids 22: 1060-
`1062; M. Akimoto et al. (1998) Appl. Biochemistry and Biotechnology 73: 269-278).
`Durch Stammselektion Ist eine Anzahl von Mutantenstammen der entsprechenden
`Mikroorganismen entWickeIt worden, die eine Reihe wflnschenswerter Verbindungen,
`einschlieBlich PUFAs, produzieren. Die Mutation und Selektion von Stammen mit
`verbesserter Produktion eines bestimmten Molekuls wie den mehrfach ungesattigten
`
`1O
`
`15
`
`20'
`
`25
`
`30
`
`35
`
`40
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO 2005/083093
`
`PCT/EP2005/001863
`
`6
`
`Fettséiuren ist jedoch ein zeitraubendes und schwieriges Verfahren. Deshalb werden,
`wann immer moglich wie oben beschrieben gentechnologische Verfahren bevorzugt.
`Mit Hilfe der vorgenannten Mikroorganismen lassen sich jedoch nur begrenzte Mengen
`der gewiinschten mehrfach ungesattigten Fettsauren wie DPA, EPA oder ARA her-
`stellen. Wobei'diese in der Regel je nach venNendeten Mikroorganismus als Fettsaure-
`gemische aus beispielsweise EPA, DPA und ARA anfallenu
`
`Hohere Pflanzen enthalten mehrfach ungesattigte Fettsauren wie Linolséure (C18:2)
`und Linolensa‘ure (C1 8. 3). ARA, EPA und DHA kommen im Samenél hoherer Pflanzen
`gar nicht oder nur in Spuren vor (E. Ucciani: Nouveau Dictionnaire des Huiles Végé—
`tales. Technique & Documentation— Lavoisier, 1995 ISBN: 2-7430-0009-0). Es wa're
`jedoch vorteilhaft, in hoheren Pflanzen, bevorzugtIn Olsaaten wie Raps, Lein, Sonnen-
`blume und Soja, LCPUFAs herzustellen, da auf diese Weise grol'se Mengen qualitativ
`hochwertiger LCPUFAS f'L'Ir die Lebensmittelindustrie, die Tierern'a'hrung und fiJr
`.
`pharmazeutische Zwecke kostengtinstig gewonnen werden kénnen. Hierzu werden
`vorteilhaftenlveise iiber gentechnische Methoden Gene, die fiir Enzyme der Biosynthe—
`se von LCPUFAs kodieren, in Olsaaten eingefflhrt und exprimiert, vorteilhaft im Samen
`exprimiert. Dies sind Gene, die beispielsweise fiJr A—6—Desaturasen, A-6—Eiongasen, A-
`5-Desaturasen, A—5—Eiongasen oder A—4-Desaturasen kodieren. Diese Gene konnen
`vorteilhaft aus Mikroorganismen und niederen Pflanzen isoliert werden, die LCPUFAs
`herstellen und in den Membranen oder Triacylglyceriden einbauen. So konnten bereits
`A—G-Desaturase—Gene aus dem Moos Physcomitrella patens und A—6-ElOngase—Gene
`aus P. patens und dem Nematoden C..elegans isoliert werden.
`
`FiJr die Synthese von Arachidons'a'ure, Eicosapentaensaure (EPA) und Docosahe—
`xaensaure (DHA) werden verschiedene Synthesewege diskutiert(Figur.1).So erfolgt
`die Produktion von EPA bzw. DHAIn marinen Bakterien wie Vibrio sp. oder Shewanel—
`la sp. nach dem Polyketid-Weg (Yu, R. et al. Lipids 35:1061-1064, 2000; Takeyama, H.
`et al. Microbiology 143:2725-2731, 1997).
`
`Ein alternative Strategie verlauft iiber die wechselnde Aktivitat von Desaturasen und
`Eiongasen (Zank, T.K. et al. Plant Journal 31:255-268, 2002; Sakuradani, E. et al.
`Gene 238:445-453, 1999). Eine Modifikation des beschriebenen Weges iiber A6-
`Desaturase, A6-Elongase, A5-Desaturase, A5-Elongase, A4-Desaturase ist der
`Sprecher—Syntheseweg (Sprecher 2000, Biochim. Biophys. Acta 1486:219—231) in
`S'a‘ugetieren. Anstelle der A4-Desaturierung erfolgt hier ein weiterer Elongationsschritt
`auf 024, eine weitere A6-Desaturierung und_ abschliessend eine B-Oxidation auf die C22-
`Kettenlénge. FI'.'Ir die Herstellung in Pflanzen und Mikroorganismen ist der sogenannte
`Sprecher-Syntheseweg (siehe Figur 1) allerd‘ings nicht geeignet, da die Regulations-
`mechanismen nicht bekannt sind.
`
`10
`
`15
`
`20
`
`25
`
`30
`
`35
`
`Die polyungeséttigten Fettsauren konnen entsprechend ihrem Desaturierungsmuster in
`zwei grorse Klassen, in w—6- oder w-3-Fettsauren eingeteiltwerden, die metabolisch
`und funktionell unterschiedlich Aktivitaten haben (Fig. 1).
`‘
`
`40
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO 2005/083093
`
`PCT/EP2005/001863
`
`7
`
`A18 Ausgangsprodukt f'L'Ir den w-64Stoffwechselweg fungiert die Fettséure Linolséure
`(18:2Ag1z), wéhrend der wu3-Weg fiber Linolenséure (18:31191215) abléuft Linolenséure
`wird dabei durch Aktivitét einer w-3—Desaturase gebildet (Tocher et al. 1998, Prog.
`Lipid Res. 37, 73-117; Domergue et al. 2002, Eur. J. Biochem 269, 4105-4113).
`
`Séugetiere und damit auch der Mensch verfugen uber keine entsprechende Desatura—
`éeaktivitét (A-12- und w-3-Desaturase) und massen diese Fettséuren (essentielle
`Fettséuren) 'L'Iber die Nahrung aufnehmen. Uber die Abfolge von Desaturase— und
`
`10
`
`Elongase-Reaktionen werden dann aus diesen Vorstufen die physiologisch wichtigen
`polyungeséttigten Fettséuren Arachidonséure (= ARA, 20:4A58111‘1),eine w-6-Fettséure
`und die beiden w—3—Fettséuren Eicosapentaen— (= EPA, 20:5A513 1111'17) und Docosahe—
`xaenséiure (DHA, 22:614'7'10'13'17'19) synthetisiert. Die Applikation von w-3-Fettséuren
`zeigt dabei die wie oben beschrieben therapeutische Wirkung bei der Behandlung von
`HeIz-Kreislaufkrankheiten (Shimikawa 2001, World Rev. Nutr. Diet. 88, 100-108),
`
`15
`
`Entzi‘mdungen (Calder 2002, Proc. Nutr. Soc. 61, 345-358) und Arthridis (Cleiand und
`James 2000, J. Rheumatol. 27, 2305-2307).
`
`Aus ernéhrungsphysiologiecher Sicht ist es deshalb g'L'Instig eine Verschiebung
`zwiechen dem w-6-Syntheseweg und dem w-3—Syntheseweg (siehe Figur 1) zu
`erreichen, so dass mehr w-3—Fettséuren hergestellt werden. In der Literatur wurden die
`enzymatischen Aktivitéten verschiedener w---3Desaturasen beschrieben, die C182-,
`C224- oder 0225-Fettséuren desaturieren (siehe Figur 1). Keine der biochemisch
`beschriebenen Desaturasen setzt jedoch ein breites Substratspektrum des w—6-
`, Synthesewegs zu den entsprechenden Fettséuren des w-3—Syntheseweg um.
`
`Die Veriéngerung von Fettséuren durch Eiongasen um 2 bzw. 4 C-Atome ist fiir die
`
`Produktion von Czo- bzw. C22-PUFAs von entscheidender Bedeutung. Dieser Prozess
`verléiufi iner 4 Stufen. Der erste Schritt stellt die Kondensation von MalonyI-CoA an
`das Feftséure—Acyl-COA durch die Ketoacyl-CoA—Synthase (KCS, im weiteren Text als
`Elongase bezeichnet). Es folgt dann ein Reduktionschritt (Ketoacyl-CoA—Reduktase,
`
`KCR), ein Dehydratationss'chritt (Dehydratase) und ein abschliessender Reduktions-
`
`schritt (enoyi-CoA-Reduktase). Es wurde postuliert, class die Aktivitéit der Elongase
`
`die Spezifitét und Geschwindigkeit des gesamten Prozesses beeinflussen (Millar and
`
`Kunst, 1997 Plant Journal 122121-131).
`
`Zur Hersteliung von DHA (C2226 n-3) in Organismen, die diese Fettséure nat'L'Iriicher-
`
`weise nicht produzieren, wurde bisher keine spezifische Elongase beschrieben. Bisher
`wurden nur Eiongasen beschrieben, die C20- bzw. 024-Fettséuren bereitstelien. Eine A—
`5—Eiongase—Aktivitét wurde bisher noch nicht beschrieben.
`
`Erste transgene Pflanzen, die fI'Jr Enzyme der LCPUFA-Biosynthese kodierende Gene
`
`enthalten und exprimieren und als Folge dessen LCPUFAs produzieren, wurden
`
`beispielsweise in DE 102 19 203 (Verfahren zur Herstellung mehriach ungeséttigter
`Fettséuren in Pfianzen) oder WO 2004/071467 beschrieben. Diese Pflanzen produzie-
`
`ren allerdings LCPUFAs in Mengen, die f'L'Ir eine Aufarbeitung der in den Pflanzen
`enthaltenen Ole noch weiter optimiert werden mUssen. So betrégt der Gehalt von ARA
`
`20
`
`25
`
`3O
`
`35
`
`40
`
`CSIRO Exhibit 1006
`CSIRO Exhibit 1006
`
`
`
`WO 2005/083093
`
`.
`
`PCT/EP2005/001863
`
`'
`
`8
`
`in den in DE-A-102 19 203 beschriebenen Pflanzen Iediglich 0,4 bis 2% und der Gehalt
`von EPA Iediglich 0,5 bis 1%, jeweils bezogen auf den Gesamtlipidgehalt der Pflanze.
`lln WO 2004/071467 werden hdhere Gehalte an mehrfach ungeséttigten Czo- und C22-
`Fettséuren, wie ARA, EPA oder DHA offenbart. Jedoch‘weist das offenbarte Verfahren
`einige gravierende Nachteile auf. DHA Iéést sich im offenbarten Verfahren offenbar
`fiberhaupt nicht im Samen nachweisen. FUr eine Herstellung von PUFAs ist Soja
`aufgrund des